28 agosto 2017
28 agosto 2017
Nesta segunda-feira (28), deve ser divulgado em Diário Oficial, a concessão da Anvisa de registro do medicamento Spiranza, usado no tratamento de pacientes com Atrofia Muscular Espinhal, conhecida como AME, que atinge em média um a cada 10 mil bebês nascidos em todo mundo. A Agência Nacional de Vigilância Sanitária divulgou a liberação do medicamento na última sexta-feira (25).
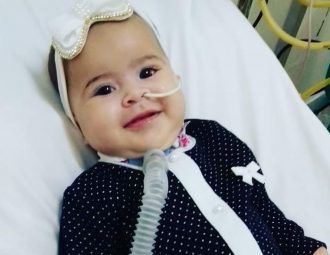
Para a mãe da bebê Lavínia Vitória Cunha, hoje com 5 meses, foi a melhor notícia recebida desde que a menina foi diagnosticada com a doença há dois meses.
“Estamos muito felizes. Essa liberação vai facilitar muito o acesso ao medicamento, acredito que os custos serão reduzidos, pelo menos”, afirma Daiane Gabriela Pereira da Cunha.
Por conta da doença degenerativa, que afeta o sistema nervoso e causa fraqueza muscular, Lavínia só respira com ajuda de aparelhos, se alimento por meio de sonda e desde os 3 meses vive no Hospital das Clínicas de Botucatu (SP). “Eu parei de trabalhar para poder ficar com ela, porque ela não tem previsão de alta, ela depende do respirador. A gente se reveza nos cuidados com a Lavínia, eu, meu pai e minha mãe.”
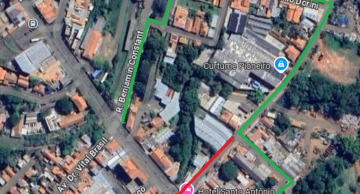
E toda esperança da família está no medicamento que, até essa liberação feita pela Anvisa, só poderia ser importado de países como os Estados Unidos. O custo do tratamento até então era de cerca de R$ 3 milhões. Para levantar essa quantia, a família iniciou uma campanha nas redes socais e também em toda a cidade com a venda de camisetas, rifas e a até uma passeata, que foi realizada neste sábado (26). Com essas iniciativas a família já conseguiu arrecadar R$ 51 mil.
“Nossa esperança é que ela possa respirar sozinha, comer, existe até a possibilidade de andar com esse tratamento, nós conhecemos outras crianças nessa situação e um deles tem um ano e já está ficando em pé com a aplicação dessas seis primeiras doses, que é uma espécie de vacina.”
Tratamento no Brasil
De acordo com nota da agência divulgada na sexta-feira , a decisão será publicada nesta segunda-feira e o remédio poderá ser adquirido como uma solução injetável e com a concentração de 2,4 mg/ml. Ele só poderá ser comercializado desta forma no Brasil.
O tratamento com a substância nusinersen (conhecida como o nome comercial de Spiranza) foi liberado nos Estados Unidos em dezembro 2016 pela FDA, agência que regula alimentos e drogas no país. Segundo a agência, o medicamento, que seria o primeiro usado no tratamento da AME, é uma terapia gênica capaz de estabilizar a morte celular de neurônios e impedir ou retardar a evolução da doença. Testes feitos em crianças nos primeiros meses de vida mostraram melhorias que vão de 40% a 60% nas condições de saúde.
No Brasil, um menino morador de Ribeirão Preto, também no estado de São Paulo, conseguiu o medicamento após um intensa campanha nas redes sociais e também na cidade. Em um mês, a família de Joaquim Marques conseguiu arrecadar o dinheiro para tratamento e o menino já tomou a primeira dose da medicação em abril deste ano.
Após a publicação oficial, a Anvisa informou que haverá um procedimento para a determinação do preço pelo governo. Sem a necessidade de compra no exterior, espera-se que o Spinraza seja vendido por um valor mais acessível no Brasil. O remédio já é comercializado nos Estados Unidos, Europa, Japão e Canadá.
A Anvisa explica que, como se trata de uma substância inédita no país, o processo foi complexo e envolveu uma avaliação crítica das informações técnicas e legais. A agência diz que impôs caráter prioritário ao registro, com aprovação cinco meses após o pedido da farmacêutica.
Fonte: Portal G1
Compartilhe esta notícia